
Фотосинтез (от греч. phos , род. падеж photos - свет и synthesis - соединение) - процесс образования
органич. соединений клетками высших растений, водорослей и нек-рых бактерий
за счёт энергии света, поглощённой пигментами (хлорофиллом, бактериохлорофиллом).
Ф.- осн. процесс в биосфере, ведущий к запасанию энергии света в виде энергии
хим. связей восстановленных соединений (углеводов), образующихся из СО2
и Н2О. Суммарное ур-ние Ф. имеет вид

т. е. в процессе Ф. образуется
молекула шестиуглеродного сахара, запасающая 112 ккал/моль, и выделяется свободный
кислород. Мир гетеротрофных организмов (большинство бактерий, животные, человек)
потребляет для своей жизни свободную энергию продуктов Ф. и выделившийся кислород.
За год на Земле образуется 150.109 т органич. вещества
и выделяется ок. 200.109 т свободного кислорода.
Ф. можно разделить на 2
стадии: световую и темновую. Основа световой стадии - система окислительно-восста-новит.
реакций, в ходе к-рых происходит поглощение фотона hv пигментами и затем
транспорт электронов по цепи переносчиков, расположенных в фотосинтетич. биол.
мембранах. Конечные продукты световой стадии Ф.- восстановленный никотинамидадениннуклеотиддифосфат
(НАДФ-Н) и аденозинтрифосфорная к-та (АТФ)- используются в темновой стадии восстановления
СО2 (ц и к л К а л ь в и н а) и образования углеводов. На рис. приведена
схема первичных процессов (световая стадия) Ф. высших растений. В них участвуют
две последоват. фото-хим. реакции, в каждой из к-рых поглощение кванта света
приводит к отрыву электрона от пигмента и восстановлению переносчиков в цепи
Ф. Этот процесс протекает в реакционных центрах (РЦ) фотосистем I и II с участием
в реакционных центрах фотоактивного пигмента (Р) - первичного донора электрона.
Фотосистема II (ФС II) обеспечивает перенос электрона от молекулы воды и восстановление
подвижного переносчика пластохинона (Пx ). Образованный при отрыве
электрона хлорофилл (Р+ ) ФС II обладает высоким окислительно-восстановит.
потенциалом (U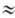 +1,0 В) и отрывает электрон у молекулы воды (U
+1,0 В) и отрывает электрон у молекулы воды (U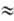 0,8
В) через систему ферментов, в результате чего выделяется кислород (в процессе
выделения одной молекулы
О2 участвуют 4 электрона). Подвижный Пх диффундирует через
мембрану и передаёт электрон через кластер, состоящий из большого числа молекул
Пх, в макромолекулярный комплекс, содержащий цитохромы f и
b6, от к-рого затем через подвижный пластоцианин Пц
электрон попадает на фотоактивный хлорофилл ФС I. Возбуждение ФС I приводит
к восстановлению акцепторной части цепи ферредоксин - НАДФ, а окисленный хлорофилл
ФС I восстанавливается от Пц.
0,8
В) через систему ферментов, в результате чего выделяется кислород (в процессе
выделения одной молекулы
О2 участвуют 4 электрона). Подвижный Пх диффундирует через
мембрану и передаёт электрон через кластер, состоящий из большого числа молекул
Пх, в макромолекулярный комплекс, содержащий цитохромы f и
b6, от к-рого затем через подвижный пластоцианин Пц
электрон попадает на фотоактивный хлорофилл ФС I. Возбуждение ФС I приводит
к восстановлению акцепторной части цепи ферредоксин - НАДФ, а окисленный хлорофилл
ФС I восстанавливается от Пц.
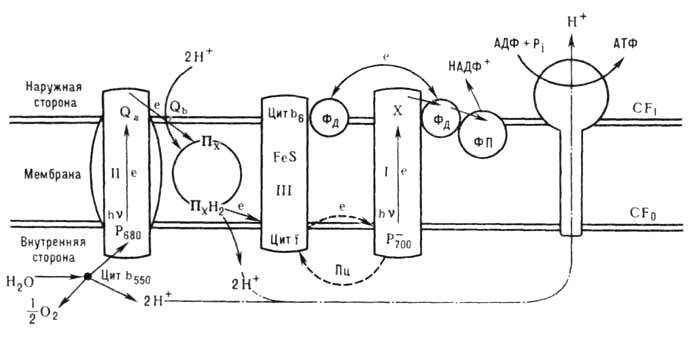
Рис. Схема световой стадии
фотосинтеза высших растений: I - комплекс фотосистемы ФС I; II - комплекс ФС
II; III - цитохром-ный b6- f-комплекс; CF1-CF0-
сопрягающий комплекс; Фд - ферредоксин, ФП - флавопротеиновая Фд
- НАДФ-редуктаза; пути транспорта электрона е обозначены стрелками; Qa
- Qb - вторичные акцепторы хинонной природы.
При переносе электрона
через мембрану по цепи переносчиков образуется трансмембранная разность эл--хим.
потенциалов Dy по обе стороны мембраны. Величина Dy включает составляющую, зависящую
от разности хим. потенциалов ионов водорода, и составляющую, зависящую от разности
электрич. потенциалов между пограничными областями мембраны, возникающей вследствие
неравномерного распределения зарядов в мембране и ионов по обе её стороны. Разность
эл--хим. потенциалов является источником энергии для образования АТФ в спец.
мак-ромолекулярных АТФ-комплексах. Центр. проблема биофизики первичных стадий
Ф. состоит в исследовании механизмов процессов миграции энергии возбуждения
между молекулами фотосинтетич. аппарата, разделения зарядов в фотоактивном пигменте
РЦ фотосистем I и II и переноса электрона по цепи Ф.
В 30-х гг. 20 в. было показано,
что выделение одной молекулы О2 после короткой (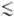 10-5
с) световой вспышки происходит за время ~0,04-0,1 с, соответствующее времени
пролёта электрона по цепи реакций от Н2О до конечных продуктов световой
стадии, и что в реакции выделения О2 участвуют ~ 300 молекул хлорофилла,
объединённых в фотосинтетич. единицу (ФСБ). Один фотон hv, поглощённый
любой молекулой хлорофилла из 300, может вызвать однократный фотохим. процесс,
если попадает в фотоактивный
пигмент (Р) в РЦ в результате миграции энергии.
10-5
с) световой вспышки происходит за время ~0,04-0,1 с, соответствующее времени
пролёта электрона по цепи реакций от Н2О до конечных продуктов световой
стадии, и что в реакции выделения О2 участвуют ~ 300 молекул хлорофилла,
объединённых в фотосинтетич. единицу (ФСБ). Один фотон hv, поглощённый
любой молекулой хлорофилла из 300, может вызвать однократный фотохим. процесс,
если попадает в фотоактивный
пигмент (Р) в РЦ в результате миграции энергии.
Т. о., РЦ являются тушителями
электронного возбуждённого
состояния пигментов Ф. Действительно, длительность существования синглетного
возбуждённого состояния
в растворе хлорофилла, измеряемая по длительности затухания
его флуоресценции, составляет t = 5.10 с. В фотосинтетич.
мембранах с активными РЦ t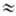 100
пс (для пигментов светособирающей антенны ФСE). В мутантах фотосинтезирующих
организмов, лишённых РЦ, значение t близко
к 4,0-4,5 пс, что указывает на отсутствие тепловой диссипации энергии при её
миграции в антенне. Детальное исследование
флуоресценции фотосинтетич.
пигментов, возбуждённых пикосекундными лазерными импульсами (см. Фемтосекундная
спектроскопия), показало наличие неск. компонент затухания флуоресценции,
к-рые отражают процессы миграции энергии по антенне, захвата энергии возбуждения
и стабилизации разделённых зарядов в РЦ. При относительно сильных взаимодействиях
между молекулами пигментов (энергия взаимодействия
100
пс (для пигментов светособирающей антенны ФСE). В мутантах фотосинтезирующих
организмов, лишённых РЦ, значение t близко
к 4,0-4,5 пс, что указывает на отсутствие тепловой диссипации энергии при её
миграции в антенне. Детальное исследование
флуоресценции фотосинтетич.
пигментов, возбуждённых пикосекундными лазерными импульсами (см. Фемтосекундная
спектроскопия), показало наличие неск. компонент затухания флуоресценции,
к-рые отражают процессы миграции энергии по антенне, захвата энергии возбуждения
и стабилизации разделённых зарядов в РЦ. При относительно сильных взаимодействиях
между молекулами пигментов (энергия взаимодействия 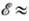 0,01 эВ), находящихся на одном белковом носителе, миграция осуществляется по
экситонному механизму. Перенос энергии по механизму индуктивного резонанса происходит
между пигментами, локализованными на разных субъединицах, напр. между светособирающим
пигментным комплексом и частью антенны, фокусирующей энергию непосредственно
на РЦ. Светособирающий белок (пигментный комплекс) может мигрировать в мембране
между ФСI и ФСII, обеспечивая их равномерное световое возбуждение. За время
существования возбуждения (~ 100-200 пс) в антенне, состоящей из 100-300 молекул
хлорофилла, экситон успевает 10-15 раз попасть в ловушку РЦ, что обеспечивает
эфф. захват возбуждения. Затем за время 1-3 пс происходят высокоэффективное
разделение зарядов
и перенос электрона на первичный акцептор. Общая схема процессов, происходящих
в РЦ, имеет вид
0,01 эВ), находящихся на одном белковом носителе, миграция осуществляется по
экситонному механизму. Перенос энергии по механизму индуктивного резонанса происходит
между пигментами, локализованными на разных субъединицах, напр. между светособирающим
пигментным комплексом и частью антенны, фокусирующей энергию непосредственно
на РЦ. Светособирающий белок (пигментный комплекс) может мигрировать в мембране
между ФСI и ФСII, обеспечивая их равномерное световое возбуждение. За время
существования возбуждения (~ 100-200 пс) в антенне, состоящей из 100-300 молекул
хлорофилла, экситон успевает 10-15 раз попасть в ловушку РЦ, что обеспечивает
эфф. захват возбуждения. Затем за время 1-3 пс происходят высокоэффективное
разделение зарядов
и перенос электрона на первичный акцептор. Общая схема процессов, происходящих
в РЦ, имеет вид
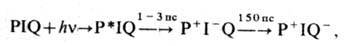
где I - первичный акцептор
порфириновой природы, Q - вторичный акцептор хинонной природы.
Последующее восстановление
Р+ происходит от вторичных доноров электрона за 10 -7-
10-6 с (тирозин в ФСII, Пц в ФСI, цитохром в бактериальном
фотосинтезе). Методы фемтосекундной спектроскопии позволяют разрешить во времени
кинетику переноса электрона в нач. период (1-3 пс) на этапе 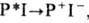 , а также проследить колебат. характер движения ядер при образовании P+I-
из комплекса Р*I.
, а также проследить колебат. характер движения ядер при образовании P+I-
из комплекса Р*I.
Важнейшие особенности транспорта
электрона в РЦ - его высокая скорость и направленность в плотном макромолекулярном
комплексе, где исключены обычные диффузионные активац. механизмы хим. реакций
в растворах по типу сталкивающихся частиц.
Данные рентгеновского
структурного анализа кристал-лич. образцов белка РЦ, а также данные, полученные
на разл. мутантах методами генной инженерии, дают полное представление о ближайшем
белковом окружении активных групп переносчиков РЦ и позволяют оценить расстояния
между ними, к-рые составляют ~0,5-1,5 нм. Эфф. механизм, обеспечивающий транспорт
электрона в РЦ,- туннельный перенос, при к-ром часть электронной энергии воспринимается
акцептирующей модой, к-рой служат колебания водорода в группах О-Н, С-Н, и рассеивается
по колебат. степеням свободы молекулы. Низкотемпературные процессы переноса
электрона в РЦ действительно наблюдаются при 100-4 К, что свидетельствует об
их туннельной природе. В ряде случаев (реакция восстановления Р+
от цитохрома f) наблюдаются нек-рое снижение скорости переноса
при понижении температуры от комнатной до 80-100 К и её независимость от температуры
при дальнейшем охлаждении образца. В др. случаях (реакция 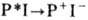 в бактериальном фотосинтезе) скорость переноса не меняется во всём диапазоне
изменения температур.
в бактериальном фотосинтезе) скорость переноса не меняется во всём диапазоне
изменения температур.
Белок также активно участвует
в формировании контактных состояний между донорно-акцепторными группами переносчиков
электрона, т. е. в создании "электронной тропы". Этот процесс связан
с внутримолекулярной кон-формац. подвижностью белков РЦ и зависит от температуры.
Действительно, параллельное изучение внутримолекулярной динамики белка методами
радиоспектроскопии (спин-зонды, g-резонансные спектрометры) показало
уменьшение скорости переноса электрона и параллельное падение внутримолекулярной
подвижности белка РЦ при понижении температуры или степени гидратации образцов.
В тех случаях, когда исходная взаимная ориентация донорно-акцепторных групп
переносчиков оптимальна, скорость переноса электрона от температуры не зависит,
а в нек-рых образцах при понижении температуры наблюдается даже её рост (в 2-3 раза).
Присоединение электрона к молекуле переносчика приводит к новой его равновесной конформации. Конформац. перестройки в белке РЦ играют регуляторную роль, обеспечивая формирование "электронной тропы" и направленный характер переноса электрона по цепи переносчиков.

Понятие же "физического вакуума" в релятивистской квантовой теории поля подразумевает, что во-первых, он не имеет физической природы, в нем лишь виртуальные частицы у которых нет физической системы отсчета, это "фантомы", во-вторых, "физический вакуум" - это наинизшее состояние поля, "нуль-точка", что противоречит реальным фактам, так как, на самом деле, вся энергия материи содержится в эфире и нет иной энергии и иного носителя полей и вещества кроме самого эфира.
В отличие от лукавого понятия "физический вакуум", как бы совместимого с релятивизмом, понятие "эфир" подразумевает наличие базового уровня всей физической материи, имеющего как собственную систему отсчета (обнаруживаемую экспериментально, например, через фоновое космичекое излучение, - тепловое излучение самого эфира), так и являющимся носителем 100% энергии вселенной, а не "нуль-точкой" или "остаточными", "нулевыми колебаниями пространства". Подробнее читайте в FAQ по эфирной физике.
|
|