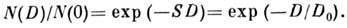
Радиационная биология - наука о действии ионизирующих излучений на биол. объекты. Поражающее действие ионизирующих
излучений обусловлено ионизацией макромолекул нуклеиновых кислот, белков
и др. Различают два пути воздействия: прямой, при к-ром энергия излучения поглощается
непосредственно в самих макромолекулах, и косвенный, при к-ром энергия
поглощается водой и низкомолекулярными соединениями, содержащимися в объекте,
а повреждение макромолекулам наносится свободными радикалами - продуктами радиолиза.
При поглощённой дозе всего лишь в 0,01 Гр (1 рад) в каждой клетке осуществляются
сотни тысяч актов ионизации в клеточных структурах [ядре, цитоплазме, мембранах
(см. Биофизика)], что приводит к множеств. нарушениям жизнедеятельности
клетки. Однако большинство нарушений преходящи и не вызывают гибели клетки.
В животном организме клетки одних тканей (кроветворные,
половых органов, слизистой кишечника) активно делятся, воспроизводя себе подобные;
клетки других тканей (почек, печени, сердца, мышц, нейроны и др.) делятся редко
или вообще не делятся. Соответственно различают два вида гибели клеток - репродуктивную
и интерфазную. Репродуктивная гибель состоит в нарушении способности делящихся
клеток к неограниченному воспроизводству: после 1-2 делений дефектные потомки
клеток отмирают. При интерфазной гибели вскоре после облучения гибнут сами облучённые
клетки. Для всех делящихся и большинства неделящихся клеток интерфазная гибель
наступает лишь при дозах в сотни Гр. Исключение составляют лимфоциты и половые
клетки на нек-рых стадиях их развития; они гибнут интерфазно уже при дозах в
неск. десятков Гр.
Причины и закономерности репродуктивной и интерфазной
гибели различны. Наиб. изучена репродуктивная гибель. Она наступает в результате
повреждения молекулы ДНК, завершающегося разрывом одной или обеих её нитей,
что препятствует дальнейшему воспроизводству нормальных клеток. Зависимость
доли клеток, сохранивших репродуктивную способность после облучения в дозе D, имеет вид
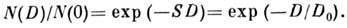
Здесь N(0) и N(D) - число клеток
до и после облучения; величина S = 1/D0 характеризует
радиочувствительность клеток, D0 - доза, снижающая
число выживших клеток в е раз. Для большинства делящихся клеток D0
= (1,2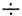 2,0)
Гр. Часто экспоненциальному участку дозовой кривой предшествует участок кривой
с меньшим наклоном (рис. 1).
2,0)
Гр. Часто экспоненциальному участку дозовой кривой предшествует участок кривой
с меньшим наклоном (рис. 1).
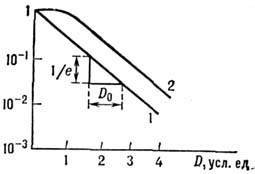
Рис. 1. Зависимость репродуктивной гибели
клеток от дозы D; по оси ординат - доля клеток, сохранивших репродуктивную
способность;
1,2 - разные формы дозовых кривых.
Радиочувствительность делящихся клеток зависит
от многих факторов и может быть искусственно увеличена (сенсибилизация) пли
уменьшена (защита); соответственно D0 уменьшается или увеличивается.
Наиб. эффективным естеств. сенсибилизатором является кислород: в его отсутствие
поражение различных биол. объектов (макромолекул, клеток, организмов в целом),
как правило, ослабляется (кислородный эффект). При этом D0
для клеток увеличивается в 3 раза. С ростом линейной плотности ионизации
радиочувствительность клеток и тканей возрастает.
Повреждение ДНК, обусловливающее репродуктивную
гибель клетки, не является для неё фатальным благодаря существованию мощных
систем восстановления (репарации). Часть возникающих в результате ионизации
первичных повреждений репарируется хим. восстановителями, присутствующими в
клетке. Осн. восстановителем является аминокислота глута-тион. Она конкурирует
с внутриклеточным кислородом, фиксирующим
первичные повреждения, и препятствует их восстановлению. Повреждения, сохраняющиеся
после этого физ--хим. этапа репарации, эффективно устраняются ферментными системами,
специфически репари-рующими разл. виды генетпч. повреждений. Конечный поражающий
эффект облучения обусловлен неотрепари-рованной частью первичных повреждений
ДНК. Доля их в обычных условиях невелика (доли %), что и обусловливает относит.
устойчивость живых клеток к действию ионизирующих излучений. С этим же связана
возможность увеличить радиочувствительность, искусственно подавляя способность
делящихся клеток к репарации, либо снизить их радиочувствительность, создавая
условия для лучшей репарации потенц. повреждении ДНК.
Механизм интерфазной гибели клеток изучен слабее,
неясна и причина резкого отличия в радиочувствительности лимфоцитов от др. видов
клеток. В отличие от репродуктивной гибели, изменения, ведущие к интерфазной
гибели, наблюдаются во всех клетках и с дозой облучения меняется не доля погибших
клеток, а ср. время гибели всей популяции (рис. 2). Причина различий, по-видимому,
в том, что интерфазная гибель обусловлена повреждением не уникальной структуры
клетки (ДНК), а мембран и др. множественных её структур.
Рис. 2. Зависимость интерфазной гибели лимфоцитов
от дозы; по оси ординат - время гибели половины облучённых клеток
(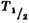 ).
).
Радиац. гибель целостного организма млекопитающих
обусловлена опустошением популяций делящихся клеток и тканей т. н. критических
органов, необходимых для жизнедеятельности. Такими органами являются кроветворные
и пищеварительные. В кроветворных органах (костный мозг, селезёнка) и тонком
кишечнике есть активно делящиеся клетки, являющиеся родоначальниками (стволовыми)
для всех функционирующих клеток крови и клеток тонкого ки-шечника, ответственных
за всасывание питательных веществ. Репродуктивная гибель стволовых клеток, снижающая
их численность ниже совместимого с жизнью критич. уровня, приводит к гибели
организма.
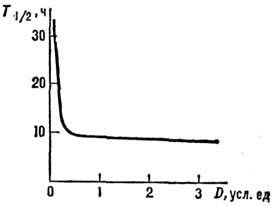
На рис. 3 приведена дозовая кривая выживаемости
млекопитающих при g-облучении всего организма. Доза летальности 50% особей
в популяции (ЛД50) различна для
млекопитающих разных видов, но форма дозовой кривой и причины гибели одинаковы.
При дозах порядка ЛД50 критической для организма является система
кроветворения, при больших дозах - слизистая оболочка тонкого кишечника. В первом
случае часть животных гибнет через 10-14 дней, во втором - через 4-7 дней после
облучения. При D > 1 Гр вплоть до абс. летальной дозы у выживших особей
наблюдается лучевая болезнь разной тяжести.
Рис. 3. Дозовая кривая гибели млекопитающих.
Существует ряд мер профилактич. защиты организма
от облучения. Наиб. эффективны два класса хим. защитных веществ (радиопротекторов)
при введении их за 10-15 мин до облучения. Это соединения, содержащие серу,-
тиолы и индолил-алкилампны. Первые, подобно внутриклеточному глутатиону, способствуют
физ--хим. репарации первичных повреждений, конкурируя с кислородом и, по-видимому,
способствуя ферментативной репарации. Вторые сужают сосуды и тем самым также
ослабляют поражающее действие кислорода в облучённых клетках критич. органов.
В нек-рых случаях необходимо увеличить радиочувствительность
клеток, напр. при радиотерапии опухолей. Сенсибилизаторами могут служить т.
н. электрон-акцепторные соединения, роль к-рых аналогична действию кислорода,
но они лучше проникают в глубь опухоли.
Помимо повреждений, проявляющихся вскоре после
облучения в больших дозах, ионизирующее излучение вызывает отдалённые последствия
(в осн. канцерогенез и генетич. нарушения), к-рые могут возникнуть при любых
дозах и характере облучения (разовом, хронич., локальном). Вероятность возникновения
отдалённых последствий возрастает с дозой, но экспериментально она определена
лишь при достаточно больших дозах. Достоверному определению её при малых дозах
препятствуют отсутствие достаточного статистич. материала и адекватных контрольных
групп животных, а главное, огромный фон аналогичных заболеваний у человека,
вызванных иными канцерогенными и мутагенными факторами окружающей среды. Поэтому
при нормировании допустимых доз облучения (см. Нормы радиационной безопасности)вероятность отдалённых последствий рассчитывают, используя линейную экстраполяцию
эффекта больших доз в область малых и при допущениях о тождественности возникающих
повреждений и возможности переноса данных с животных на человека.
Среди патологич. изменений, вызываемых облучением
в живых организмах, встречаются такие, к-рые являются полезными для человека.
Напр., под действием определ. доз облучения в нек-рых случаях на растениях наблюдается
т. н. стимуляционный эффект (более раннее созревание, увеличение зелёной массы,
накопление полезных продуктов обмена веществ и т. п.). Практич. значение имеет
облучение с целью выведения полезных мутантов растений, бактерий (напр., вырабатывающих
пенициллин) и др. Поражающее действие используется в радиотерапии зло-качеств.
опухолей, а также для стерилизации лекарств, препаратов и перевязочных материалов,
дезинсекции зерна, предотвращения прорастания картофеля и др. В научных исследованиях
биол. действие радиации применяется для определения размеров макромолекул, вирусов
и бактерий, изучения топографии радиочувст-вит. структур в клетке, исследования
процессов миграции энергии в белках и нуклеиновых кислотах, выяснения роли отд.
клеточных образований в эмбриогенезе и др.
Развитие Р. б. привело к появлению самостоятельных её направлений: радиационной генетики, радиационной микробиологии, радиоэкологии, космич. Р. б. и др.

Л. X. Эйдус
|
|