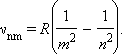 |
Источником формирования подтасовочной и алогичной теории Бора явился простейший из атомов - атом водорода, параметры которого к моменту формирования Нильсом Бором своей модели уже были хорошо изучены экспериментально, и эмпирические формулы, описывающие различные параметры атома водорода уже были получены И. Бальмером, И. Ридбергом, М. Планком, Ф. фон Ленардом и др.. Он содержит единственный электрон. Ядром атома является протон – положительно заряженная частица, заряд которой равен по модулю заряду электрона, а масса в 1836 раз превышает массу электрона. Еще в начале XIX века были открыты дискретные спектральные линии в излучении атома водорода в видимой области (так называемый линейчатый спектр) и закономерности, которым подчиняются длины волн (или частоты) линейчатого спектра, были хорошо изучены количественно (И. Бальмер, 1885 г.). Совокупность спектральных линий атома водорода в видимой части спектра была названа серией Бальмера. Позже аналогичные серии спектральных линий были обнаружены в ультрафиолетовой и инфракрасной частях спектра. В 1890 году И. Ридберг получил эмпирическую формулу для частот спектральных линий:
|
Для серии Бальмера m = 2, n = 3, 4, 5, ... . Для ультрафиолетовой серии (серия Лаймана) m = 1, n = 2, 3, 4, ... . Постоянная R в этой формуле называется постоянной Ридберга. Ее численное значение R = 3,29·1015 Гц. До Бора механизм возникновения линейчатых спектров и смысл целых чисел, входящих в формулы спектральных линий водорода (и ряда других атомов), оставались непонятными. Постулаты Бора определили направление развития новой науки – квантовой физики атома. Но они не содержали рецепта определения стационарных состояний (орбит) и соответствующих им значений энергии En, а также нарушали законы электромагнетизма Максвелла и постулат СТО о конечности скорости света, на что последователи "копенгагенсокй школы" просто не обращали внимания. Правило квантования, приводящее к правильным, согласующимся с опытом значениям энергий стационарных состояний атома водорода, было угадано Бором. Бор предположил, что момент импульса электрона, вращающегося вокруг ядра, может принимать только дискретные значения, кратные постоянной Планка. Для круговых орбит правило квантования Бора записывается в виде:
|
Здесь me – масса электрона, v – его скорость, rn – радиус стационарной круговой орбиты. Правило квантования Бора позволяет вычислить радиусы гипотетических стационарных орбит электрона (который на самом деле неподвижен, что следует из химических свойств соединений) в атоме водорода и определить значения энергий. Воображаемую скорость электрона, вращающегося по круговой орбите некоторого радиуса r в кулоновском поле ядра, можно было получить из второго закона динамики, определив ее соотношением:
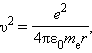 |
где e – элементарный заряд, ε0 – электрическая постоянная. Скорость электрона v и радиус стационарной орбиты rn связаны правилом квантования Бора. Отсюда следует, что радиусы воображаемых стационарных круговых орбит (воображаемых, - так как реально, как это уже было понятно из модели Резерфорда, при движении электрона по орбите он стал бы излучать, и ни о какой стационарности не могло быть и речи) можно было определить выражением
|
Самой близкой к ядру орбите соответствует значение n = 1. Радиус первой орбиты, который называется боровским радиусом, равен
|
Радиусы последующих орбит возрастают пропорционально n2. Полная механическая энергия E системы из атомного ядра и электрона, обращающегося по стационарной круговой орбите радиусом rn, равна
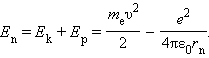 |
Следует отметить, что Ep < 0, так как между электроном и ядром действуют силы притяжения. Подставляя в эту формулу выражения для v2 и rn, получим:
|
Целое число n = 1, 2, 3, ... называется в квантовой физике атома главным квантовым числом. Согласно второму постулату Бора, при переходе электрона с одной стационарной орбиты с энергией En на другую стационарную орбиту с энергией Em < En атом испускает квант света, частота νnm которого равна ΔEnm / h:
|
Эта формула в точности совпадает с эмпирической формулой Ридберга (выведена из нее Бором) для спектральных серий атома водорода, если положить постоянную R равной
|
Подстановка числовых значений me, e, ε0 и h в эту формулу дает результат
| R = 3,29·1015 Гц, |
который очень хорошо согласуется с эмпирическим значением R. Рис. 1 иллюстрирует образование спектральных серий в излучении атома водорода при переходе электрона с высоких стационарных орбит на более низкие.
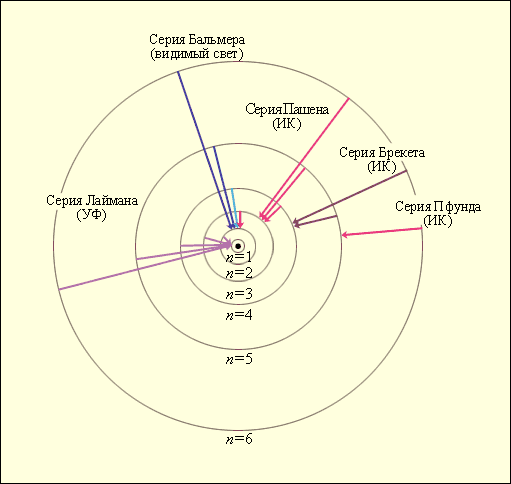 |
| Рисунок 1. Стационарные орбиты атома водорода и образование спектральных серий. |
На рис. 2. изображена диаграмма энергетических уровней атома водорода и указаны переходы, соответствующие различным спектральным сериям.
 |
| Рисунок 2. Диаграмма энергетических уровней атома водорода. Показаны переходы, соответствующие различным спектральным сериям. Для первых пяти линий серии Бальмера в видимой части спектра указаны длины волн. |
Прекрасное согласие боровской теории атома водорода с экспериментом (иначе не могло быть, так как его формулы выведены путем подбора из эмпирических формул, полученных ранее из эксперимента) послужило веским аргументом для "копенгагенцев", в пользу теории Бора (не обращая внимания на "бревно в глазу": противоречие с теорией электромагнетизма). В связи с подтасовочностью модели Бора попытки применить его теорию к более сложным атомам не увенчались успехом. Бор не смог дать физическую интерпретацию правилу квантования.
Десятилетием позже Луи Де Бройль еще более запутал ситуацию в атомной физике, предположив абсурдное: элементарные частицы вещества (электрона, в частности) есть одновременно и объекты (весомые частицы), и процессы (волны). На основе введенных им представлений о волновых свойствах частиц Де Бройль предложил, что каждая орбита в атоме водорода соответствует волне, распространяющейся по окружности около ядра атома и абсолютно не рассеивающейся в окружающее пространство. Стационарная орбита возникает в том случае, когда волна непрерывно повторяет себя после каждого оборота вокруг ядра. Другими словами, стационарная орбита соответствует круговой стоячей волне де Бройля на длине орбиты (рис. 3). Это явление очень похоже на стационарную картину стоячих волн в струне с закрепленными концами (за исключением необходимого условия: такого "закрепления" или иных материальных границ, могущих создать стоячую волну в реальном атоме нет).
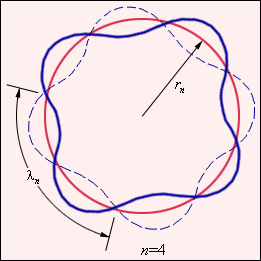 |
| Рисунок 3. Иллюстрация идеи де Бройля возникновения стоячих волн на стационарной орбите для случая n = 4. |
В стационарном квантовом состоянии атома водорода на длине орбиты должно укладываться по идее де Бройля целое число длин волн λ, то есть
| nλn = 2πrn. |
Подставляя в это соотношение длину волны де Бройля λ = h / p, где p = mev – импульс электрона, получим:
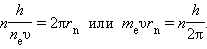 |
Таким образом, - решил Де Бройль, - боровское правило квантования связано с волновыми свойствами электронов. Успехи теории Бора в объяснении спектральных закономерностей в изучении атома водорода превратили во всеобщую сенсацию. Атом теперь представлялся квантово-волновой системой, где материя "растворилась" в волнах, а волны стали всем (это при том, что наличие физической среды, которая бы "волновалась" и создавала эти волны, отрицалось. Это были волны - фантомы, волнующиеся сами в себе, без физической среды, в которой реализуется любое реальное колевание, или часто только в математических и даже математико-статистических формулах, как к примеру у Шрёдингера, который в свойственном ему духе издевательства над логикой, представлял электрон в виде "облака верояности").
Так как к моменту появления теории Бора было уже экспериментально установлено, что энергетические уровни стационарных состояний атомов дискретны, то теория Бора была провозглашена прозорливой. На самом деле дискретность ("квантованность") состояний энергии атома была продемонстрирована в опыте Д. Франка и Генриха Герца уже в 1913 г. В нем исследовалось столкновение электронов с атомами ртути. Оказалось, что если энергия электронов меньше 4,9 эВ, то их столкновение с атомами ртути происходит по закону абсолютно упругого удара. Если же энергия электронов равна 4,9 эВ, то столкновение с атомами ртути приобретает характер неупругого удара, то есть в результате столкновения с неподвижными атомами ртути электроны полностью теряют свою кинетическую энергию. Это означает, то атомы ртути поглощают энергию электрона и переходят из основного состояния в первое возбужденное состояние,
| E2 – E1 = 4,9 эВ. |
Согласно боровской концепции, при обратном самопроизвольном переходе атома ртуть должна испускать кванты с частотой
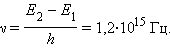 |
Спектральная линия с такой частотой действительно была обнаружена в ультрафиолетовой части спектра в излучении атомов ртути.
Представление о дискретных состояниях найденных экспериментально Франком и Герцем противоречило планетарной модели Резерфорда. Поэтому возник вопрос, не опровергает ли квантовая теория законы классической физики? Квантовая физика не отменила фундаментальных классических законов сохранения энергии, импульса, электрического разряда, но модель Бора противоречила электромагнетизму Максвелла. Согласно провозглашенному Нильсом Бором, но не выполненному им в своей модели "принципу соответствия", квантовая физика должна включать в себя законы классической физики, и при определенных условиях можно обнаружить плавный переход от квантовых представлений к классическим. Как считали "копенгагенцы", это можно было видеть на примере энергетического спектра атома водорода (рис. 2), в котором при больших квантовых числах n >> 1 дискретные уровни постепенно сближаются, и возникает плавный переход в область непрерывного спектра, характерного для классической физики. Однако при этом, они опять же закрывали глаза на нарушение законов электромагнетизма внутри атома.
Половинчатая, "полуклассическая" и "достаточно сумасшедшая" (нарушавшая законы логики и электромагнетизма) теория Бора явилась тем тупиком, в котором атомная физика застряла на целое столетие. Этому помог своими тоже "достаточно сумасшедшими" математическими моделями (впрочем, искаженно переписанными волновыми уравнениями Гельмгольца и других физиков XIX века) Эрвин Шрёдингер.
Он заявил, что физический смысл имеет только вероятность обнаружить электрон в том или ином
месте, описываемая квадратом модуля волновой функции |Ψ|2. Волновая функция Ψ
является решением основного уравнения квантовой механики – "уравнения
Шредингера". Оказалось, что состояние электрона в атоме характеризуется целым
набором квантовых чисел. Главное квантовое число n определяет квантование
энергии атома. Для квантования момента импульса вводится так называемое
орбитальное квантовое число l. Проекция момента импульса на любое
выделенное в пространстве направление (например, направление вектора  магнитного поля) также принимает дискретный ряд значений. Для
квантования проекции момента импульса вводится магнитное квантовое число m.
Квантовые числа n, l, m связаны определенными правилами квантования. Например,
орбитальное квантовое число l может принимать целочисленные значения от 0 до
(n – 1).
магнитного поля) также принимает дискретный ряд значений. Для
квантования проекции момента импульса вводится магнитное квантовое число m.
Квантовые числа n, l, m связаны определенными правилами квантования. Например,
орбитальное квантовое число l может принимать целочисленные значения от 0 до
(n – 1).
Магнитное квантовое число m может принимать любые целочисленные значения в интервале ±l. Таким образом, каждому значению главного квантового числа n, определяющему энергетическое состояние атома, соответствует целый ряд комбинаций квантовых чисел l и m.
Путая совершенно разные вещи: физическую реальность и её ощущение, измерение в конкретном эксперименте, которое есть лишь отражение реальности, но не сама реальность, Шрёдингер решил, что каждой комбинации квантовых чисел соответствует определенное распределение вероятности |Ψ|2 обнаружения электрона в различных точках пространства («электронное облако верояности»), которое якобы и есть сама физическая реальность. Состояния, в которых орбитальное квантовое число l = 0, описывались им сферически симметричными распределениями вероятности. Их назвали s-состояниями (1s, 2s, ..., ns, ...). При значениях l > 0 сферическая симметрия электронного облака нарушается. Состояния с l = 1 называются p-состояниями, с l = 2 – D-состояниями и т. д. На рис. 4 изображены кривые распределения вероятности ρ(r) = 4πr2|Ψ|2 обнаружения электрона в атоме водорода на различных расстояниях от ядра в состояниях 1s и 2s.
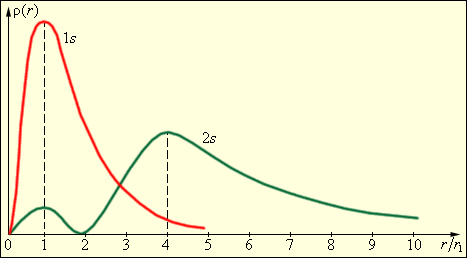 |
| Рисунок 4. Распределение вероятности обнаружения электрона в атоме водорода в состояниях 1s и 2s. r1 = 5,29·10-11 м – радиус первой боровской орбиты. |
Как видно из рис. 4, электрон в состоянии 1s (основное состояние атома водорода) может быть обнаружен на различных расстояниях от ядра. С наибольшей вероятностью его можно обнаружить на расстоянии, равном радиусу r1 первой боровской орбиты. Вероятность обнаружения электрона в состоянии 2s максимальна на расстоянии r = 4r1 от ядра. В обоих случаях атом водорода Шрёдингер представлял в виде сферически симметричного электронного облака вероятности, в центре которого находится ядро. При этом он "забыл", что вероятность не есть сущность физического мира, но лишь понятие внутри стохастической модели в мозгу, на бумаге (в формулах) или вычислительном устройстве. Таким жульническим методом была произведена подмена реальной физики "клиническими", "достаточно сумасшедшими" моделями. "Достаточность сумасшествия" определяется фатальным нарушением логики в этих построениях.
Когда тот или иной физик использует понятие "физический вакуум", он либо не понимает абсурдности этого термина, либо лукавит, являясь скрытым или явным приверженцем релятивистской идеологии.
Понять абсурдность этого понятия легче всего обратившись к истокам его возникновения. Рождено оно было Полем Дираком в 1930-х, когда стало ясно, что отрицание эфира в чистом виде, как это делал великий математик, но посредственный физик Анри Пуанкаре, уже нельзя. Слишком много фактов противоречит этому.
Для защиты релятивизма Поль Дирак ввел афизическое и алогичное понятие отрицательной энергии, а затем и существование "моря" двух компенсирующих друг друга энергий в вакууме - положительной и отрицательной, а также "моря" компенсирующих друг друга частиц - виртуальных (то есть кажущихся) электронов и позитронов в вакууме.
Однако такая постановка является внутренне противоречивой (виртуальные частицы ненаблюдаемы и их по произволу можно считать в одном случае отсутствующими, а в другом - присутствующими) и противоречащей релятивизму (то есть отрицанию эфира, так как при наличии таких частиц в вакууме релятивизм уже просто невозможен). Подробнее читайте в FAQ по эфирной физике.
|
|